COVID-19/インフルエンザ A&B 直接検出のための迅速免疫測定法
COVID-19/インフルエンザ A&B 直接検出用迅速免疫測定法、
COVID-19/インフルエンザ A&B 直接検出のための迅速免疫測定法,
製品詳細
使用目的
SARS-CoV-2 およびインフルエンザ A/B 抗原コンボ迅速検査キット (側方クロマトグラフィー) は、SARS-CoV-2 またはインフルエンザ A が疑われる患者の診断を支援するために、臨床症状およびその他の臨床検査結果と組み合わせて使用されます。 /B感染。この検査は医療専門家のみが使用できます。これは初期のスクリーニング検査結果のみを提供するものであり、SARS-CoV-2 またはインフルエンザ A/B 感染の確認を得るには、より具体的な代替診断方法を実行する必要があります。業務用のみ。
試験原理
SARS-CoV-2 およびインフルエンザ A/B 抗原コンボ迅速検査キット (ラテラル クロマトグラフィー) は、ラテラル フロー クロマトグラフィー免疫測定法です。Windows では 2 つの結果が得られます。左側は SARS-CoV-2 抗原。ニトロセルロースメンブレンには、「T」テストラインと「C」コントロールラインの2つのプレコートラインがあります。右側は FluA/FluB の結果ウィンドウで、ニトロセルロース膜上に「T1」FluA テストライン、「T2」FluB テストライン、「C」コントロールラインの 3 つのプレコートラインがあります。
主な内容
提供されるコンポーネントを表に示します。
| 商品名 | 猫。いいえ | サイズ | 検体 | 貯蔵寿命 | トランス。&Sto.温度 |
| SARS-Cov-2 & インフルエンザ A&B 抗原迅速検査キット (イムノクロマトグラフィーアッセイ) | B005C-01 | 1テスト/キット | 鼻咽頭スワブ、中咽頭スワブ | 24ヶ月 | 2~30℃ / 36~86℉ |
| B005C-05 | 5 つのテスト/キット | ||||
| B005C-25 | 25 テスト/キット |
操作の流れ
- ステップ 1: サンプリング
患者の頭を後ろに 70 度傾けます。綿棒が鼻の奥に届くまで慎重に鼻孔に挿入します。分泌物を吸収するために綿棒を各鼻孔に 5 秒間放置します。
- ステップ 2: テスト

1. 切り込みを引き裂いて、キットから抽出チューブを取り出し、フィルムバッグからテストボックスを取り出します。水平面に置きます。
2. サンプリング後、スミアをサンプル抽出バッファーの液面より下に浸し、回転させて 5 回押します。スミアの浸漬時間は少なくとも 15 秒です。
3. 綿棒を取り外し、チューブの端を押して綿棒内の液体を絞り出します。綿棒を生物学的有害廃棄物に投げ込みます。
4. ピペットカバーを吸引チューブの上部にしっかりと固定します。次に、抽出チューブをゆっくりと 5 回回します。
5. 2 ~ 3 滴 (約 100 μl) のサンプルをテストバンドのサンプル表面に移し、タイマーを開始します。注: 凍結サンプルを使用する場合、サンプルは室温でなければなりません。
- ステップ 3: 読書
15 分後、結果を視覚的に読み取ります。(注意: 20 分後には結果を読まないでください!)
結果の解釈
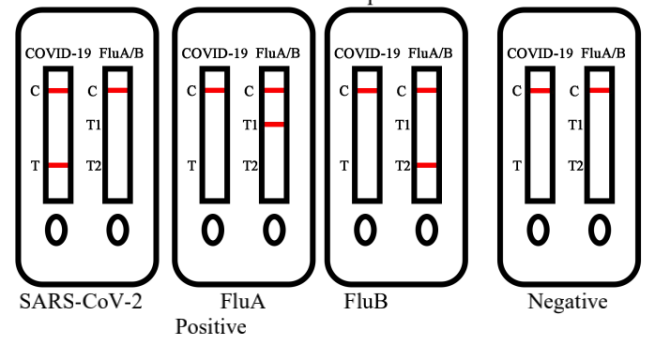
1.SARS-CoV-2 陽性結果
テスト ライン (T) とコントロール ライン (C) の両方に色のバンドが表示されます。それは、
検体中の SARS-CoV-2 抗原の陽性結果。
2.インフルエンザ陽性結果
テスト ライン (T1) とコントロール ライン (C) の両方に色のバンドが表示されます。それは、
検体中の FluA 抗原の陽性結果。
3.インフルエンザB陽性結果
テスト ライン (T2) とコントロール ライン (C) の両方に色のバンドが表示されます。それは、
検体中の FluB 抗原の陽性結果。
4.陰性結果
制御線 (C) にのみ色の帯が表示されます。それは、
SARS-CoV-2 および FluA/FluB 抗原の濃度が存在しないか、または
検査の検出限界以下です。
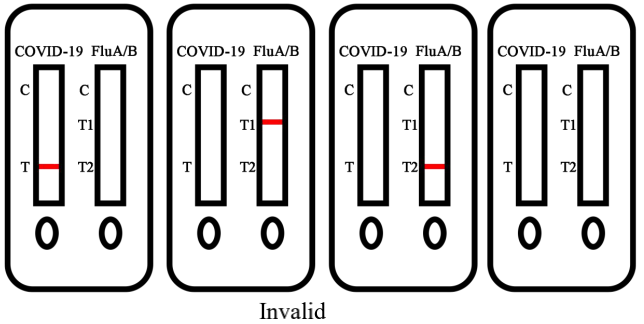
5.無効な結果
テストの実行後、コントロール ラインに目に見える色のバンドは表示されません。の
指示に正しく従わなかったか、テストに問題があった可能性があります。
悪化した。検体を再検査することをお勧めします。
注文情報
| 商品名 | 猫。いいえ | サイズ | 検体 | 貯蔵寿命 | トランス。&Sto.温度 |
| SARS-CoV-2 & インフルエンザ A/B 抗原コンボ迅速検査キット (側方クロマトグラフィー) | B005C-01 | 1テスト/キット | 鼻咽頭スワブ | 18ヶ月 | 2~30℃ / 36~86℉ |
| B005C-05 | 5 つのテスト/キット | ||||
| B005C-25 | 25 テスト/キット |
COVID-19/インフルエンザ A&B テストは、インビトロでの迅速かつ同時の定性検査を目的としたラテラルフローイムノアッセイです。
SARS-CoV-2、インフルエンザ A および/またはインフルエンザ B からのヌクレオカプシド抗原を前部から直接検出および識別
呼吸器ウイルス感染が疑われる個人から採取した鼻または鼻咽頭ぬぐい液検体
症状の発症から最初の 5 日以内に、医療従事者が新型コロナウイルス感染症と一致していると判断した場合。臨床症状と
SARS-CoV-2 とインフルエンザによる呼吸器ウイルス感染症の症状は似ている可能性があります。検査は研究所に限定される
1988 年の臨床検査改善修正 (CLIA)、42 USC §263a に基づいて認定されており、
中程度、高度、または免除された複雑さのテストを実行するための要件。この製品はポイントオブケアでの使用が認可されています
(POC)、つまり、CLIA の権利放棄証明書、準拠証明書、または証明書に基づいて運営されている患者ケア現場
認定。